Ionengitter / Salze Und Ionengitter Erklart Inkl Ubungen Ionen bilden einen festen ionenverband

Kann mir jemand die Ionenbildung erklären (evtl mit Beispiel)? (Schule, Chemie, Ionen)
Was ist eine Ionenbindung? Eine Ionenbindung ist eine chemische Bindung, die durch die Anziehung von positiv geladenen Ionen (Kationen) und negativ geladenen Ionen (Anionen) entsteht. Diese entsteht, wenn ein Atom Elektronen an ein anderes Atom abgibt oder aufnimmt, um eine stabile Elektronenkonfiguration zu erreichen. 2.

Ionengitter / Salze Und Ionengitter Erklart Inkl Ubungen Ionen bilden einen festen ionenverband
Eine Ionenbindung ist eine elektrostatische Wechselwirkung zwischen Ionen. Das bedeutet, dass sich Ionen, also Kationen und Anionen, gegenseitig anziehen. Die Ionenbindung ist die stärkste Bindung, die zwischen Teilchen herrschen kann. Erfüllung der Oktettregel Alle Atome wollen die Oktettregel erfüllen.
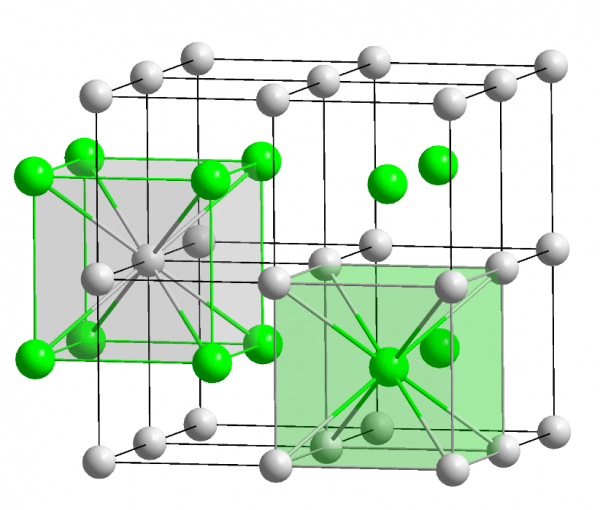
Bildung des Ionengitters Chemiewiki
Ein Ionengitter ist die regelmäßige, dreidimensionale Anordnung von positiv und negativ geladenen Ionen in einem Salz. Durch elektrostatische Anziehungskräfte halten sich die Ionen im Gitter zusammen, was Salzen ihre typische feste Struktur und hohe Schmelzpunkte verleiht. Videos anschauen Übungen starten Arbeitsblätter anzeigen Lehrer* innen

Gitterstrukturen sehr einfach erklärt 1a Technikermathe
Chemische Bindung. Unter einem Ionenkristall oder Ionengitter versteht man in der Chemie und der Festkörperphysik die regelmäßige räumliche Anordnung von Anionen und Kationen eines homogenen Stoffes im festen Zustand. Der Zusammenhalt des Gitterverbandes erfolgt durch die Ionenbindung.
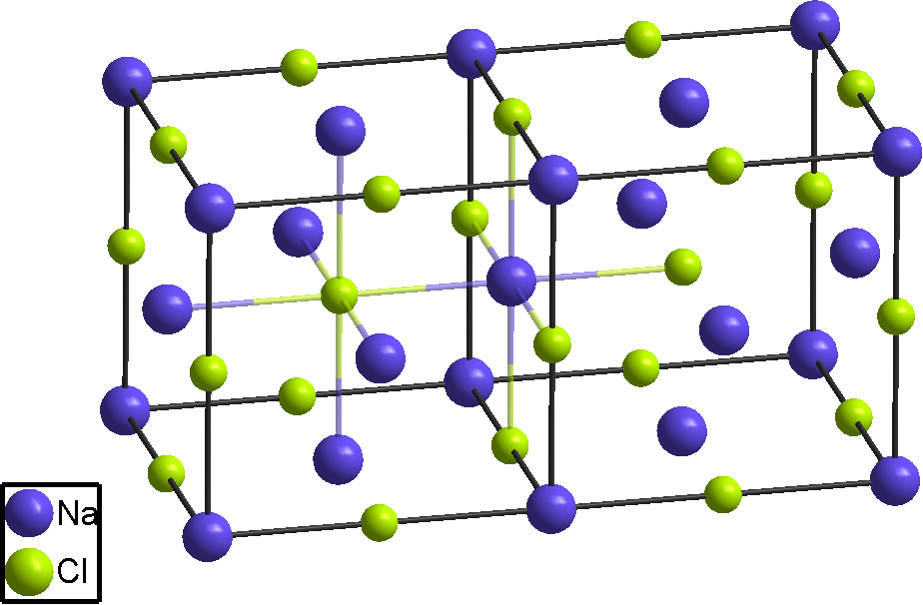
Wichtige Salze und ihre Bedeutung online lernen
Erklärung der Größe. Die Gitterenergie gibt an, wie viel Energie man benötigt, um ein Ionengitter aufzuspalten und anschließend die einzelnen Ionen in den gasförmigen Aggregatzustand zu bringen. Die Gitterenergie wird in Kilojoule je Mol \frac {\text {kJ}} {\text {mol}} molkJ angegeben. Es wird also angegeben, wie viel Kilojoule Energie.

Pin auf Learning Level Up Lernvideos
Ein Ionengitter ist eine gleichmäßige Aufstellung, die aus positiv (Kationen) und negativ (Anionen) geladenen Ionen besteht. Durch ihre entgegengesetzten Ladungen ziehen sie sich gegenseitig an und bilden eine Struktur, die wie ein Gitter aussieht: das Ionengitter.

Pin auf Learning Level Up Screens
Ein Ionengitter ist die regelmäßige Anordnung von negativ geladenen Anionen und positiv geladenen Kationen. Das Ionengitter wird von Ionenbindungen zusammengehalten. Bildung eines Ionengitters Damit Atome die Oktettregel erfüllen, bilden sie Ionen. Es gibt zwei verschiedene Arten: die Kationen und die Anionen.
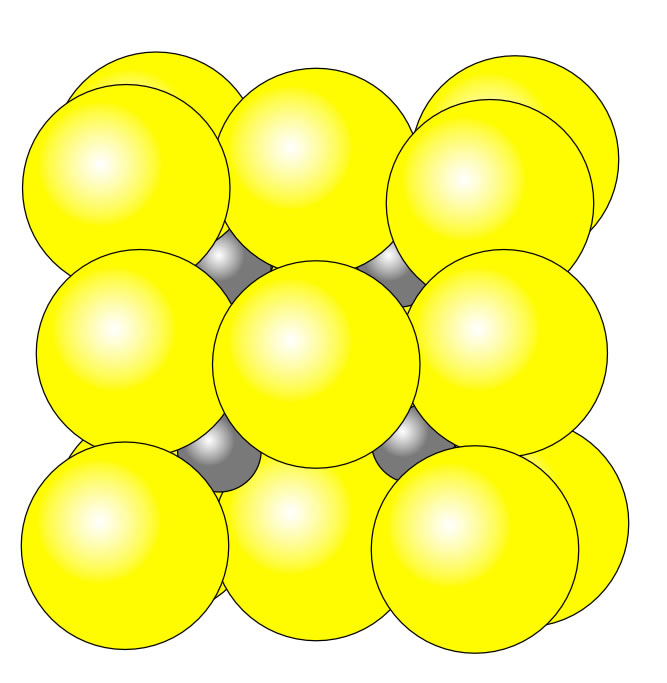
Ionengitter Chemie Fur Mediziner Chemische Bindung Chemgapedia / ionengitter ionenkristall
Unter einem Ionengitter oder Ionenkristall versteht man in der Chemie und der Festkörperphysik die regelmäßige räumliche Anordnung von Anionen und Kationen in einem homogenen Stoff im festen Zustand. Der Zusammenhalt des Gitterverbandes erfolgt durch Ionenbindungen.
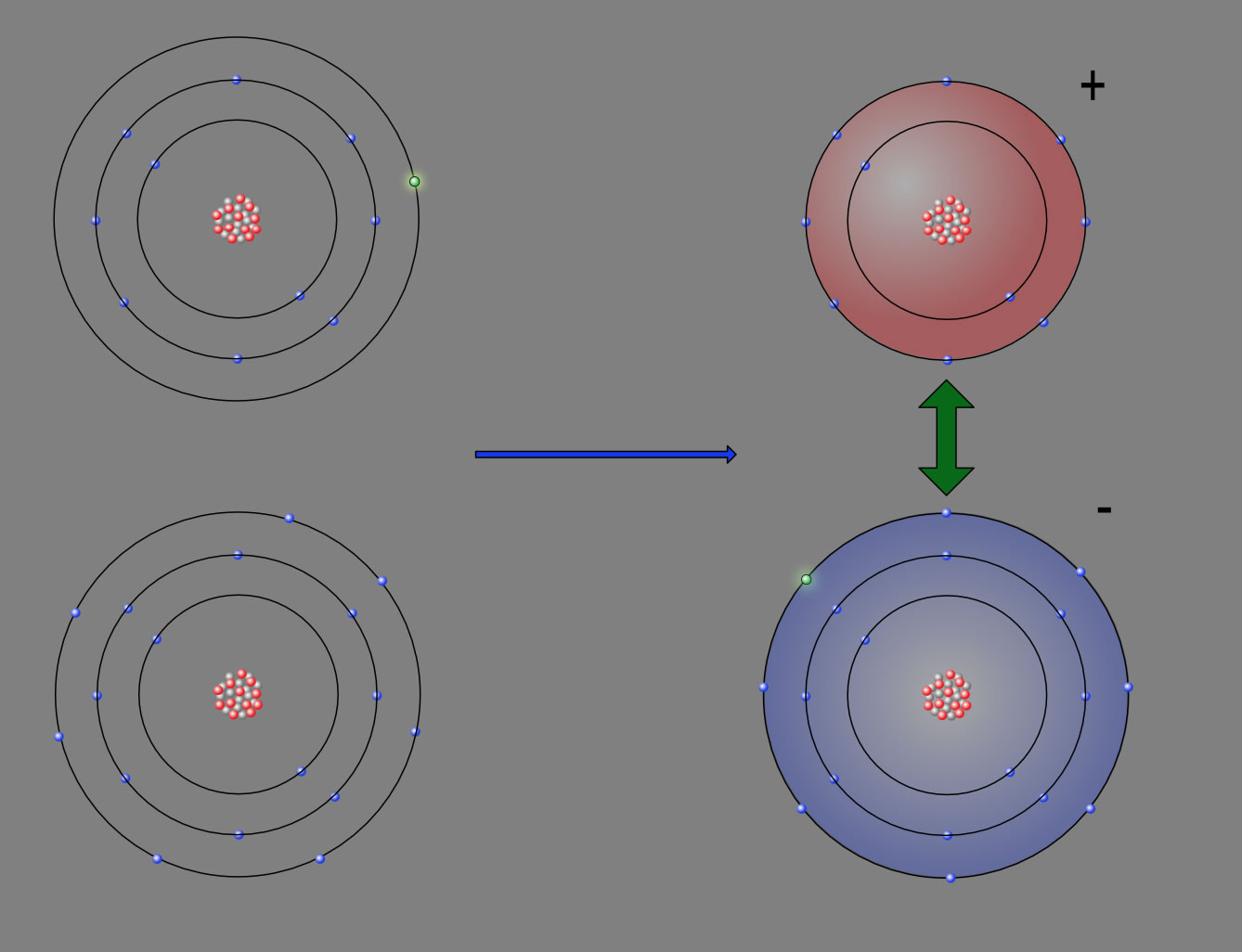
Die Ionenbindung
Aufbau des Ionengitters. Ein Ionengitter wird aus Kationen und Anionen aufgebaut, dabei stehen die Anionen und Kationen so im Verhältnis zueinander, dass das Prinzip der elektrischen Neutralität (Salze sind i.d.R ungeladen) erfüllt wird. Dabei spielt das Verhältnis der Radien von Kationen und Anionen eine entscheidende Rolle.

1.3.2 Ionenbindung _main.utf8
Bildung des Ionengitters. Wenn sich Ionen verbinden,entsteht ein Ionengitter, da sich die gleichgeladenen Ionen abstossen und die gegengleichgeladenen Ionen anziehen. Somit ist die Bildung des Ionengitters eigentlich eine Optimierung, denn die gleichgeladenen Ionen versuchen möglichst weit voneinander entfernt zu sein, während die.
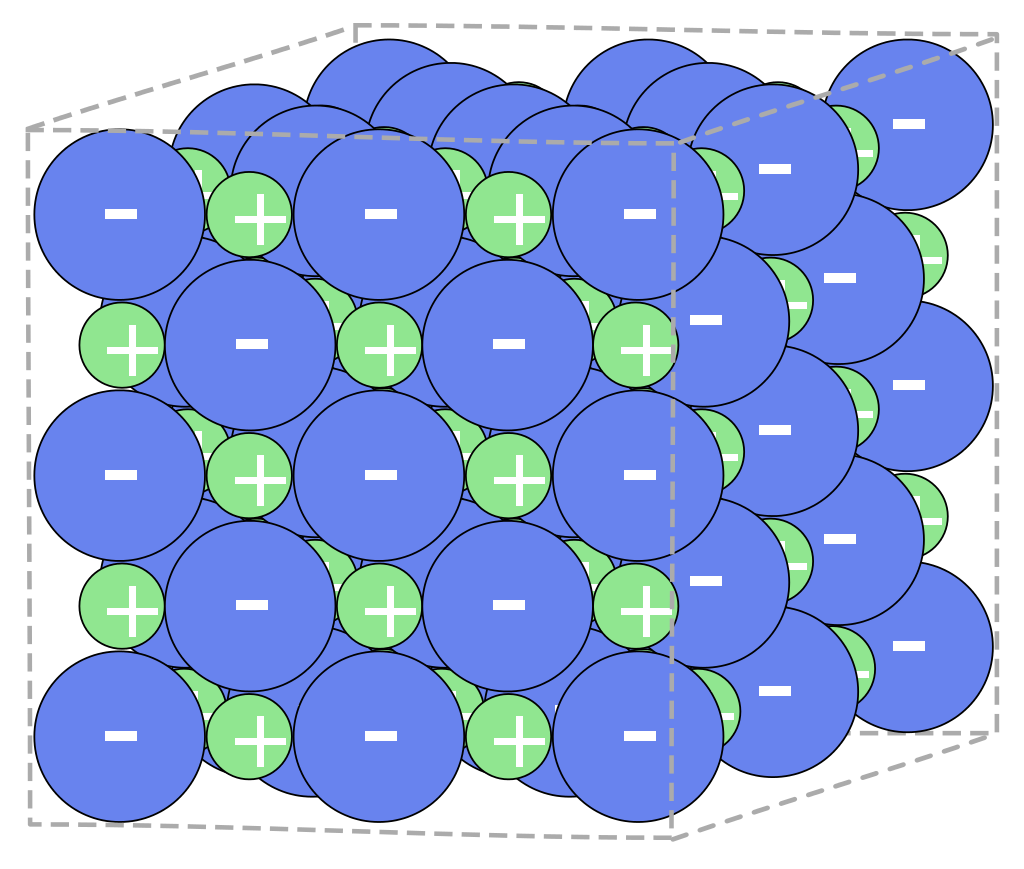
Ionenbindung lernen mit Serlo!
Unter einem Ionengitter versteht man in der Physik und Chemie die regelmäßige räumliche Anordnung von Kationen und Anionen in einem homogenen Feststoff. Der Zusammenhang innerhalb des Gitterverbandes wird durch ungerichtete Ionenbindungen gewährleistet.
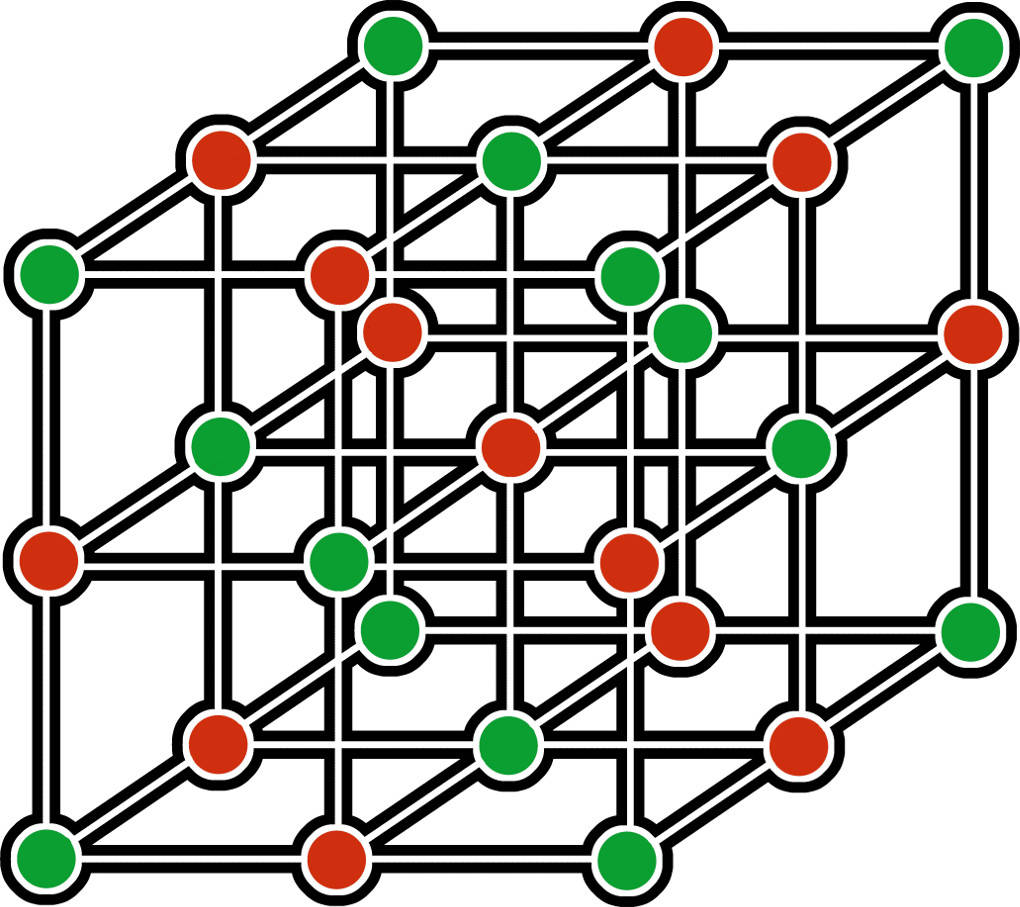
Salze Eigenschaften und Bildung online lernen
Unter einem Ionenkristall oder Ionengitter versteht man in der Chemie und der Festkörperphysik die regelmäßige räumliche Anordnung von Anionen und Kationen eines homogenen Stoffes im festen Zustand. Der Zusammenhalt des Gitterverbandes erfolgt durch die Ionenbindung.
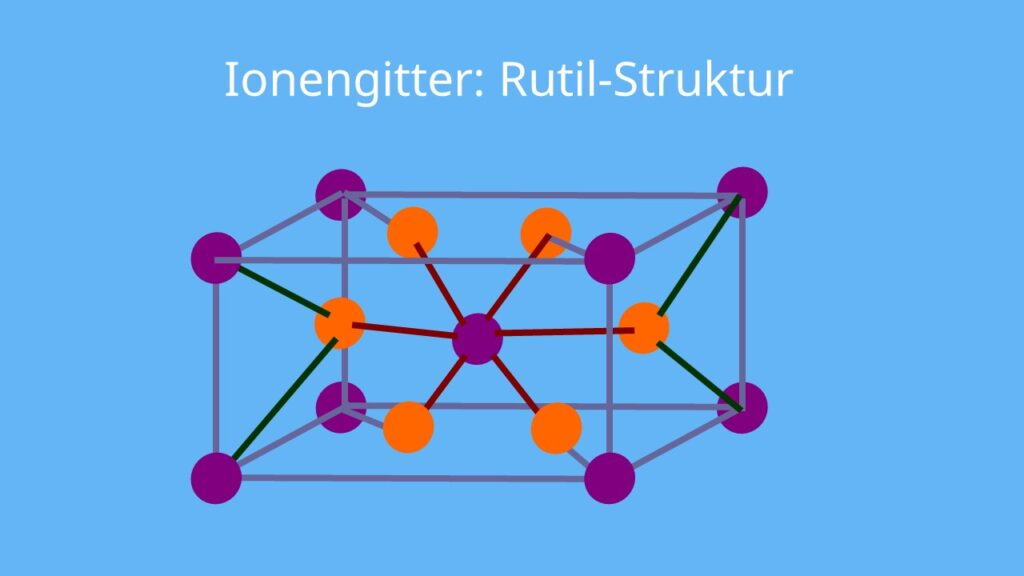
Ionengitter • einfach erklärt, Eigenschaften und Beispiele · [mit Video]
Ionengitter. Kristallographie. Chemische Bindung. jedes Atom hat sechs direkte Nachbarn. Unter einem Ionengitter oder Ionenkristall versteht man in der Chemie und der Festkörperphysik die regelmäßige räumliche Anordnung von Anionen und Kationen in einem homogenen Stoff im festen Zustand.
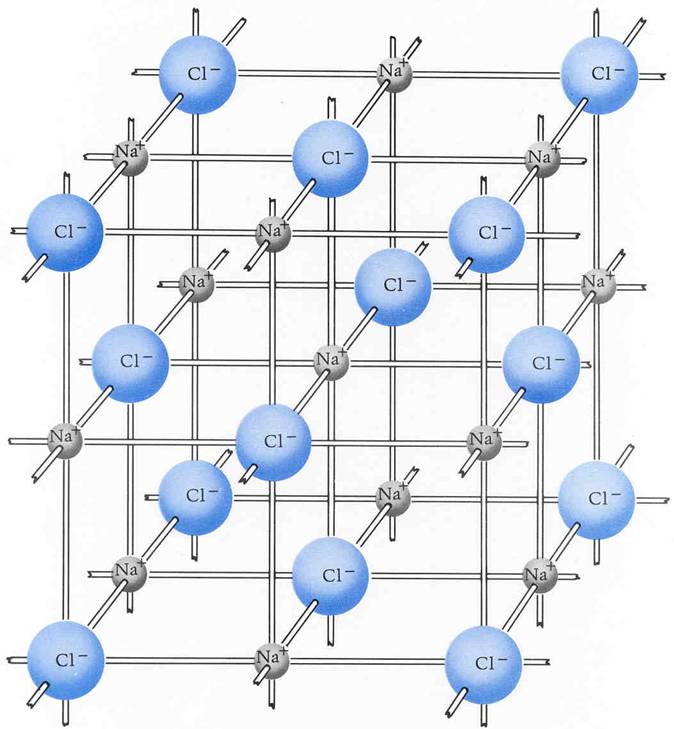
Referat Die Ionenbindung
Was ist Gitterenergie? Die Gitterenergie (Gitterdissoziationsenergie) ist die Energie, um ein Ionengitter zu zerlegen und Ionen in gasförmigen Zustand zu bringen. Die Einheit ist kJ/mol. Was ist der Unterschied zwischen Gitterenergie und Gitterenthalpie?

IonenbindungIonenKationen und Anionen YouTube
Die Definition eines Ionengitters Ein Ionengitter liegt nun vor, wenn sich die Ionen innerhalb des Stoffes gitterförmig anordnen. Ionen - eine einfache Erklärung aus der Physik lonen sind essentielle Bestandteile der Physik und der Chemie. Es handelt sich um geladene.
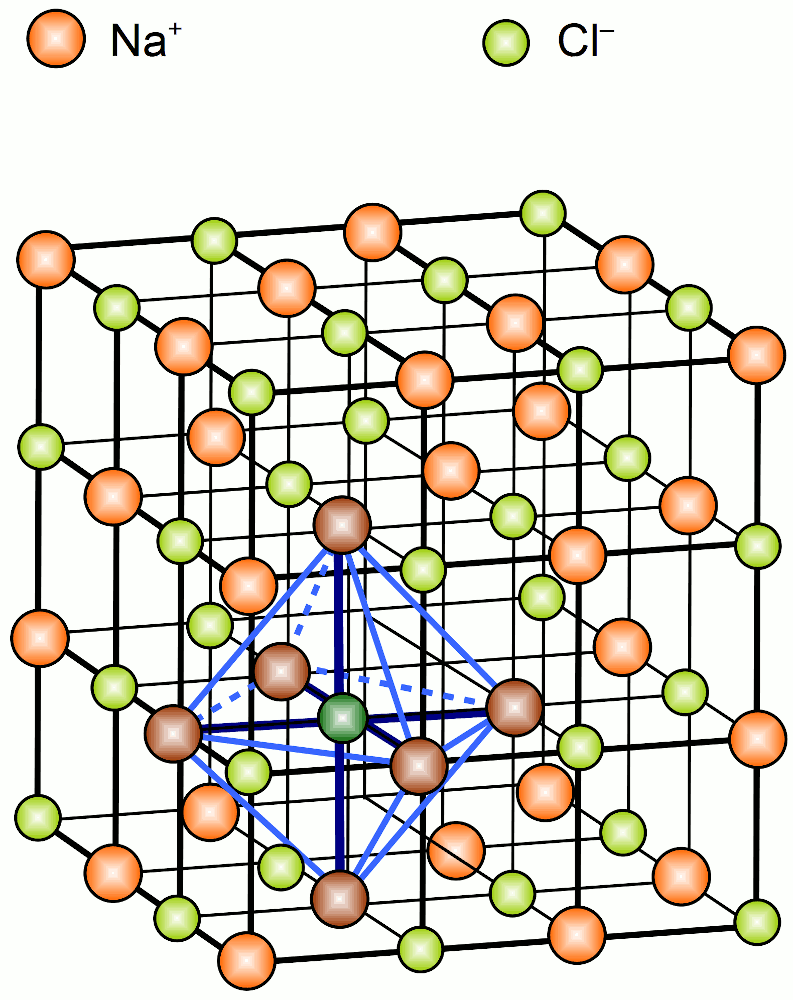
Ionengitter Chemie Fur Mediziner Chemische Bindung Chemgapedia / ionengitter ionenkristall
Die Lehre der Kristalle nennt man Kristallographie. Erklärung anhand des Kochsalzgitters (ein Ionengitter) Ionengitter: Regelmäßige Anordnung von Ionen in einem Kristall Kochsalz ( Natriumchlorid) besteht aus Natriumionen (Na+ positiv geladen) und Chloridionen (Cl-, negativ geladen).